Оценка клинических эффектов агонистов альфа2-адренорецепторов -медетомидина и ксилазина в рандомизированном двойном слепом исследовании
УДК 599.742.73.13.574.577.57.089.26
Старокожева Я.К. (ВЦ «Астин» ИП Беликов И.Н.), Климов П.В. (ООО НПО «Апи-Сан»)
Ключевые слова: ксилазин, медетомидин, собаки, кошки, агонист альфа2-адренорецепторов, кардиоваскулярные эффекты, седация.
Keywords: xylazine, medetomidine, dog, cat, alpha 2 -adrenoreceptor agonists, sedation, cardiovascular
Реферат
В двойном слепом рандомизированном исследовании изучали клинические эффекты агонистов альфа2-адренорецепторов (альфа2-агонистов) медетомидина и ксилазина во время анестезии 68 кошек и 25 собак. Для обеспечения оптимального уровня седации потребовалось 974,95± 140,07 мкг ксилазина на 1 кг массы тела и 45,81±5,35 мкг медетомидина на 1 кг массы тела животного по действующему веществу (ДВ). Ксилазин и медетомидин вызывают снижение фракции сократимости через 15 минут после введения. В группе 1, получавшей ксилазин, амплитуда изменений артериального давления в периоде 0 – 15 мин характеризовалось большим значением, чем в группе 2, которым применяли медетомидин: на 14,36% против 4,32% соответственно. Во время анестезии у всех животных регистрировали урежение дыхательных движений, однако эти изменения не были клинически значимыми. На 15 минуте после введения альфа2-агонистов у животных отмечалась гипотермия, быстрее всего она развивалась у кошек, получавших ксилазин. Визуально во время проведения операций у животных фиксировали и другие нежелательные эффекты. При применении ксилазина тремор отмечали у 41,8%, медетомидина – у 8% животных, возбуждение во время индукции и на выходе: в 23,2% и 6% случаев соответственно, рвоту в 7% и 10% случаев.
Введение
Агонисты альфа2-адренорецепторов порядка 40 лет разрешены для ветеринарного применения в странах ЕС, Канада, США, хотя первые родоначальники этого класса использовались в медицине в качестве препаратов для лечения гипертонии и патологий ЦНС. Для агонистов альфа-2-адренорецепторов были открыты такие клинические эффекты как анальгезия, анксиолизис, седация, миорелаксация, которые легли в основу их последующего широкого применения в ветеринарии как для иммобилизации диких экзотических животных [4,7], так и в хирургии домашних животных [14,16,17,20,22]. Помимо указанных клинических эффектов, введение ксилазина или медетомидина приводит к значительному уменьшению количества инъекционной и ингаляционной анестезии, необходимой для индукции и поддержания анестезии. Агонисты альфа2-адренорецепторов также ослабляют реакцию стресса при травме, снижая уровень катехоламинов и кортизола в крови после операции [3,11,20]. Достаточно подробно описаны негативные клинические эффекты для агонистов альфа2-адренорецепторов у различных видов животных. В связи с этим применение их имеет ограничение у пожилых животных, у пациентов, имеющих в анамнезе проблемы со стороны сердечно-сосудистой системы [2,6,8,9,12-14,16,17,22].
Медетомидин и ксилазин – наиболее часто используемые агонисты альфа2-адренорецепторов в хирургической и анестезиологической практике в России у мелких домашних животных, поэтому изучение клинических эффектов воздействия их на организм животных представляется интересным.
Целями данного исследования были определить и оценить основные клинические эффекты, наблюдаемые после введения рандомизированных образцов медетомидина и ксилазина у клинически здоровых собак и кошек на основании данных физиологического мониторинга, проводимого в интраоперационных условиях.
Материалы и методы
Перед началом проведения исследовательской работы флаконы с препаратом, содержащим агонист альфа2-адренорецептора: медетомидин или ксилазин предварительно рандомизировали. Для интерпретации полученных результатов, при обработке готовых данных группа животных, которым применяли образец, содержащий ксилазин – была обозначена как группа 1 (к), а медетомидин – группа 2 (м) соответственно. Согласно общепринятым рекомендациям по применению агонистов альфа2-адренорецепторов в анестезиологии животных из исследования были исключены особи, имеющие в анамнезе поражение почек, печени и сердечно-сосудистые патологии, а также животные старше 8 лет по этическим мотивам, а также во избежание неоправданного риска. Животных подбирали в группы по принципу пар-аналогов (различия не более 10 – 20 %). Образец препарата, содержащего 0,1% медетомидина гидрохлорида был предоставлен ООО НПО «Апи-Сан», Россия. В качестве опытного образца препарата, содержащего ксилазин в 0,2% концентрации, использовали препарат, произведенный компанией Interchemie Werken «de Adelaar» BV. Подготовленные образцы были переданы в многопрофильный ветеринарный центр «Астин», Московская обл. для проведения исследования в трех подразделениях компании.
Анестезиологический предоперационный осмотр проводили согласно принятым методикам, руководствуясь оценкой пациентов по шкале Американского Общества Анестезиологов (ASA) от 1 (клинически здоровый) до 5 (в критическом состоянии) [5]. Всего в исследовании участвовало 93 особи, из них 68 кошек и 25 собак обоего пола. Для индукции применялся пропофол 1%, при болезненных операциях для обеспечения анальгезии проводилась анестезия с лидокаином гидрохлоридом 2% в эпидуральное пространство, для осуществления гипнотического эффекта и поддержания анестезии применяли изофлюран, в других случаях - смесь тилетамина гидрохлорида и золазепама гидрохлорида в ИПС.
Для оценки кардиологических изменений использовали пособие [1].
Для мониторинга анестезиологического пациента применялись монитор пациента IM-10 или IM-12, Zoomed, наркозно-дыхательный аппарат DIXION Практик 3000, УЗ-аппарат Mindray DC-N6 и Mindray DC-N7 для кардиологического обследования, портативный ветеринарный тонометр марок PetMap Graphic и PetMap Graphic II.
Регистрацию данных состояния животного во время анестезии проводили на: 0 (предоперационных период) мин, 15 мин, 30 мин и 45 мин. Статистическую обработку данных проводили по методике Стьюдента с применением пакета программного обеспечения Microsoft Office Excel 2013. Во всех процедурах статистического анализа p>95.
Результаты и обсуждение
Образцы препаратов с ксилазином и медетомидином применяли согласно утвержденной инструкции. Независимо от пола и вида, в среднем для обеспечения необходимого уровня седации во время операции потребовались следующие дозы агонистов альфа2-адренорецепторов: в группе 1 (к) - 974,95± 140,07 мкг/кг массы тела и в группе 2 (м) - 45,81±5,35 мкг/кг (Рис 1.)
Рис. 1 Средние дозы препаратов агонистов альфа2-адренорецепторов, используемые для премедикации животных по ДВ.
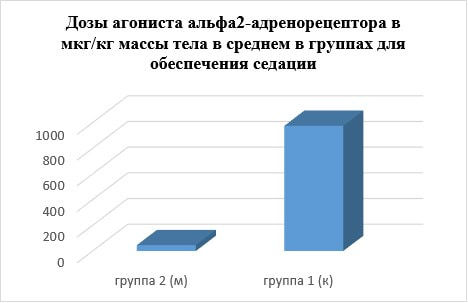
При этом для животных, находящихся в состоянии гипервозбуждения (стресс, агрессия) дополнительное введение агониста альфа2-адренорецептора не потребовалось, что опровергает устойчивое утверждение, что для высоко возбудимых животных требуется дополнительное введение седативного препарата в премедикации.
Наибольшую клиническую значимость при интраоперационном физиологическом мониторинге пациентов представляют кардиоваскулярные эффекты во время анестезии при использовании агонистов альфа2-адренорецепторов [17]. Оценить степень депрессивного влияния на миокард позволяет нам параметр фракции сократимости (ФС). В таблице 1 приведены данные по измерению параметра в первые 15 минут операции.
Таблица 1. Измерение ФС в группах (М±m, p>95)
| Параметры | Группа 1 (к) | Группа 2 (м) | ||
| 0 мин | 15 мин | 0 мин | 15 мин | |
| ФС: собаки | 46,95± 3,22 | 35,57± 4,16 | 42,47± 5,99 | 25,83± 3,54 |
| ФС: кошки | 49,78± 2,77 | 31,14±4,14 | 50,07± 2,48 | 29,18± 2,53 |
Как мы видим из данных таблицы 1, ФС у собак и кошек снижается как в группе, получавшей медетомидин гидрохлорид так и в группе животных, седированных ксилазином. И первой и во второй группе мы наблюдали среди кошек критически низкие значения ФС <15 через 15 минут после инъекции. Можно сделать предположение, что кошки более чувствительный вид, кроме того, чем ниже исходное значение ФС у животных, тем выше вероятность критического падения этого параметра и проявления так называемого «смоки эффекта». Влияние альфа2-агонистов на сократимость и сердечный выброс были описаны также в [9,12,17,18]. Также было доказано, что снижение сердечного выброса при применении альфа2-агонистов никоим образом не влияет на перфузию жизненно-важных органов у животных [17]. Механизм этого явления (снижение ФС) до сих пор не достаточно изучен, но считается, что депрессивное влияние селективных альфа2-агонистов на сердце можно снять введением атипамезола [6]. Также отмечаем, что случаев развития атриовентрикулярных блокад I и II в опытных группах мы не выявляли [18].
Альфа2-агонисты замедляют сердечные сокращения [6]. В опытных группах через 15 минут после инъекции снижение ЧСС было на 18,5-33,3%, что вполне укладывалось в физиологические параметры для вида.
Альфа2-агонисты оказывают периферическое действие на адренорецепторы в гладкой мускулатуре сосудов, вызывая вазоконстрикцию. Резкое увеличение периферического сосудистого сопротивления оказывает нагрузку на миокард. По некоторым данным [19] введение альфа2-агонистов не оказывает существенного негативного влияния на величину артериального давления (Таблица 2).
Таблица 2. Измерение величины АД, мм рт. ст. в группах (М±m, p>95)
| Группы | 0 мин, АД с/д | 15 мин, АД с/д | 30 мин, АД с/д | |||
| Группа 1 (к) | 175,55± 9,75 | 110,42± 6,75 | 150,33± 11,25 | 100,36± 10,44 | 139,03± 9,39 | 89,64± 6,66 |
| Группа 2 (м) | 175,95± 11,62 | 108,23± 8,55 | 168,35± 10,08 | 112,56± 8,41 | 158,10± 10,71 | 108,12± 10,39 |
В группе 1 (к) дельта изменений АД характеризовалось большим значением, чем в группе 2 (м): на 15 минуте АД систолическое снизилось на 14,36% по отношению к исходному значению, измеренному в предоперационный период, а в группе 2 (м) лишь на 4,32%. Хотя, как мы видим, параметры АД в предоперационном периоде практически идентичны в группах. Параксизмально резкое повышение АД (кратковременная гипертония) ˃ 200 мм. рт. ст. определяли лишь у 4 кошек из группы 1 (к) на 15 минуте и у 3 кошек и 1 собаки в группе 2 (м). Обратное гипертонии – гипотензия (<60-80 мм рт. ст.) не наблюдали у опытных животных на протяжении всего периода наблюдения.
Известно, что у седированных животных замедляется частота дыхательных движений (ЧДД), степень дыхательной депрессии прямо пропорциональна дозе вводимого альфа2-агониста [8,10]. Сравнение показателей ЧДД в группах на Рис.2.
Рис. 2 Мониторинг изменения ЧДД
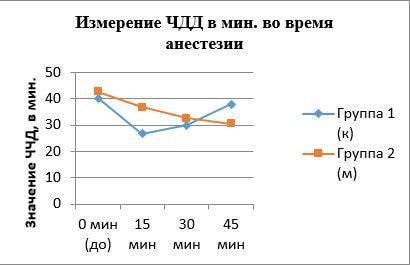
Снижение величины ЧДД через 15 минут после премедикации (Рис. 2) у животных из группы 1 (к) более резкое, в группе 2 (м) – плавное, обусловленное введением пропофола, угнетающего дыхательный центр в гипоталамусе. Во время проведения анестезии - апное наблюдали у 1 кошки в группе 1(к), в группе 2(м) случаев остановки дыхания не было. Не отмечали для альфа2-агонистов в группах эффекты гипоксемии и цианоза у животных. Оксигенация (SpO2) не опускалась ниже <89% во время операции. Определение скорости наполняемости капилляров после их сдавливания в ротовой полости не выявило статистически значимых отклонений в группах.
Во время выполнения хирургических манипуляций у анестезированных животных не редко можно определить гипотермию. Чаще у маловесных особей, теряющих тепло быстрее. Результаты измерения t°C тела животных до и во время анестезии в таблице 3.
Таблица 3. Термометрия животных в группах (M±m, p>95)
| Время, мин | 0 | 15 | 30 | 45 | |
| Группы | |||||
| Группа 1 (к) кошки | 38,49±0,14 | 37,96±0,26 | 37,75±0,28 | 37,62±0,29 | |
| Группа 1 (к) собаки | 38,49±0,26 | 37,88±0,33 | 37,76±0,28 | 38,07±0,40 | |
| Группа 2 (м) кошки | 38,54±0,16 | 38,24±0,20 | 37,80±0,21 | 37,05±0,33 | |
| Группа 2 (м) собаки | 38,68±0,32 | 37,95±0,46 | 37,54±0,33 | 37,6±0,90 |
Снижение температуры тела животного <38°С определяют, как гипотермию. На 15 минуте как видно из таблицы в группе 1 (к) собаки и кошки перешли этот рубеж, в то время как температура тела кошек в группе 2 (м) оставалась чуть выше пороговых 38°С. К 30 минуте у животных первой и второй групп диагностировали слабую гипотермию и для животных использовали грелку.
Визуально во время проведения операций фиксировали появление у животных рвоты, тремора или возбуждения во время премедикации, индукции или на выходе из анестезии. Основные побочные эффекты агонистов альфа2-адренорецепторов схематично показаны на Рис. 3.
Рис. 3. Инцидентность нежелательных явлений во время анестезии у животных
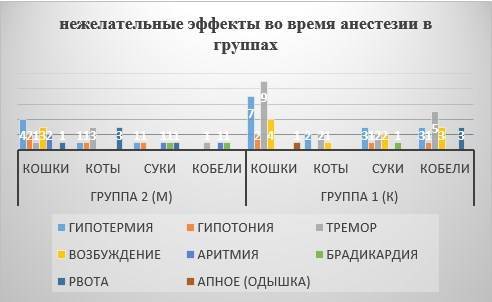
Как видно на Рис. 3 основные побочные эффекты агонистов альфа2-адренорецепторов – медетомидина и ксилазина сходны, однако большое значение имеет вероятность и частота развития тех или иных нежелательных клинических эффектов у животных во время анестезии. В группе 1 (к) случаи рвоты, тремора, возбуждения и гипотермии встречались чаще.
В целом, как и следовало ожидать медетомидин и ксилазин как агонисты альфа2-адренорецепторов оказывали сходное влияние на организм животных. Однако, нельзя не отметить, что для достижения одного и того же уровня седации, нагрузка на организм животного, которому применяли медетомидин в 20 раз меньше, чем при применении ксилазина. С некоторыми нежелательными эффектами пришлось столкнуться в 3 раза чаще при применении ксилазина. Хотя тремор, возбуждение и рвота не являются угрожающими состояниями для животного. Мониторинг пациентов по основным жизненно важным параметрам не выявил грубых отличий в воздействии ксилазина и медетомидина на организм животных, однако для последнего характерна большая «плавность» и постепенность индуцированных им изменений, без выраженных колебаний и отклонений, что может говорить о лучшей управляемости и контролируемости процесса индукции и выхода из анестезии.
Литература
1. Эхокардиография в двухмерном и М-режиме у собак и кошек. Пособие для ветеринарных врачей общей практики, Бун Дэни. Пер. с англ. Сарабьева Е.В., под редакц. Корнеева О.А. – М: Аквариум, 2015 - 94 С.
2. Adams H.R. Veterinary pharmacology and therapeutics. 8th edition. Blackwell Publishing Professional, p.313-424, 2001.
3. Benson GJ, Grubb TL, Neff-Davis C, et al. Perioperative stress response in the dog: effect of pre-emptive administration of medetomidine. Vet Surg. 2000;29:85–91.
4. Brenner G, Klopp A, Deason L, et al. Analgesic potency of alpha adrenergic agents after systemic administration in amphibians. J Pharmacol Exp Ther 1994; 270:540–545.
5. Chris Seymour, Tanya Duke. BSAVA Manual of Feline and Canine Anaesthesia and Analgesia. 2nd edition. 2007.
6. Flacke W, Flacke J, Bloor B et al. (1993) Effects of dexmedetomidine on systemic and coronary haemodynamics in the anesthetized dog. J Cardiothorac Vasc Anesth 7, 41–49.
7. Gerardo A J, Francisca A A, Cunningham A A. Comparison of chemical immobilization methods in wild foxes (pseudalopex griseus and pseudalopex culpaeus) in Chile. Journal of Wildlife Diseases, 46(4), 2010, pp. 1204–1213. Wildlife Disease Association, 2010
8. Hammond R.A., G.C.W. England. The effect of medetomidine premedication upon propofol induction and infusion anaesthesia in the dog. Vet Anaest Analg, Vol 21, Issue 1, p.24–28, July 1994
9. Haskins SC, Patz JD, Farver TB. Xylazine and xylazine ketamine in dogs. Am J Vet Res 1986;47: p. 636–641.
10. Ko JCH, Bailey JE, Pablo LS, Heaton-Jones TG. Comparison of sedative and cardiorespiratory effects of medetomidine and medetomidine-butorphanol combination in dogs. Am J Vet Res 1996;57:535–540.
11. Ko JCH, Mandsager RE, Lange DN, et al. Cardiorespiratory responses and plasma cortisol concentrations in dogs treated with medetomidine before undergoing ovariohysterectomy. J Am Vet Med Assoc. 2000 Oct 1;217(7):988-9.
12. Kuusela E., et all. Clinical effects and pharmacokinetics of medetoidine and its enantiomers in dogs. // J VetPharmacol Therap., 2000; 23: 15—20.
13. Lammintausta R. The alpha-2 adrenergic drugs in veterinary anaesthesia. 4th Proc Int Cong Vet Anaes 1991:3–8.
14. Lemke K.A. Perioperative use of selective alpha-2 agonists and antagonists in small animals. Can Vet J. 45(6): 475–480, June 2004
15. Lumb WV, Jones EW. Preanesthetics and Anesthetic Adjuncts. In: Thurmon JC, Tranquilli WJ, Benson GJ, eds. Veterinary Anesthesia. 3rd Edition. Philadelphia: Williams and Wilkins, 1996:183–209.
16. Melissa D. Sinclair. A review of the physiological effects of α2-agonists related to the clinical use of medetomidine in small animal practice A review of the physiological effects of α2-agonists related to the clinical use of medetomidine in small animal practice. Can Vet J. 2003 Nov; 44(11): 885–897.
17. Murrell J С, Hellebrekers L J. Medetomidine and dexmedetomidine: a review of cardiovascular effects and antinociceptive properties in the dog. Veterinary Anaesthesia and Analgesia, 2005, 32, 117–127.
18. Pypendop B, Verstegen JP. Hemodynamic effects of medetomidine in the dog: a dose titration study. Vet Surg 1998;27: p. 612–622.
19. Vainio O, Palmu L. Cardiovascular and respiratory effects of medetomidine in dogs and influence of anticholinergics. Acta Vet Scand 1989;30:401–408.
20. Vaisanen M, Raekallio M, Kuusela E, et al. Evaluation of the perioperative stress response in dogs administered medetomidine or acepromazine as part of the preanesthetic medication. Am J Vet Res. 2002;63:969–975.
21. Virtanen R. Pharmacological profiles of medetomidine and its antagonist, atipamezole. Acta Vet Scand Suppl. 85:29-37. 1989.
22. Young L, Brearley J, Richards D et al. (1990) Medetomidine as a premedicant in dogs and its reversal by atipamezole. J Small Anim Pract 31, 554–559.
EVALUATION OF THE CLINICAL EFFECTS OF ALPHA-2-ADRENOEPEPTOR AGONISTS (MEDETOMIDINE AND XYLAZINE) IN RANDOMIZED INVESTIGATION
Starokozheva Ya.K. (VC "Astin" IP Belikov I N), Klimov P.V. (Open Company NPO "Api-san")
SUMMERY
It was double-blind randomized study clinical effects of alpha2-adrenoreceptors (alpha2-agonists) medetomidine and xylazine during anesthesia of 68 cats and 25 dogs. To ensure the optimal level of sedation was 974.95 ± 140.07 μg of xylazine per 1 kg of b. w. and 45.81 ± 5.35 μg of medetomidine per 1 kg of b. w. of the animal. Xylazine and medetomidine induced decrease of cardiac output after15 minutes administration. In group 1 (xylazine) the amplitude of changes in blood pressure in the period 0-15 minutes was characterized by a greater value than in group 2, which injected medetomidine: 14.36% against 4.32%, respectively. During anesthesia, respiratory movements were recorded in all animals, but these changes were not clinically significant. At 15 minutes after the administration of alpha2-agonists, hypothermia was noted in animals, most rapidly it developed in cats on xylazine. Visually, during the operation, other undesirable effects were recorded in the animals. When xylazine was used, tremor was noted in 41.8% against medetomidine - 8% of animals, excitation during induction and in output: in 23.2% and 6% of cases respectively, vomiting in 7% and 10% of cases.
Статья опубликована: Журнал «Вопросы нормативно-правового регулирования в ветеринарии» №4-2017


ВНИМАНИЕ! Названия препаратов приведены в информационных целях. Любые лекарства допустимо давать питомцу только по назначению ветеринарного врача.

