УДК 619.615.038.636.8
Изучение переносимости препарата «ГАБИТАБС» (габапентин) при применении у кошек
Шантыз А.Х., доктор ветеринарных наук, профессор кафедры биотехнологии, биохимии и биофизики, shah_8383@mail.ru
Лысенко Ю.А., доктор биологических наук, доцент, профессор кафедры биотехнологии, биохимии и биофизики, yuraduban45@mail.ru
Костянко Н.О., аспирант, diesel1301@mail.ru
Хахов Л.А., кандидат ветеринарных наук, заведующий кафедрой терапии и фармакологии, shah_8383@mail.ru
ФГБОУ ВО «Кубанский государственный аграрный университет им. И.Т. Трубилина», г. Краснодар
Петрова О.В., кандидат ветеринарных наук, специалист по фармаконадзору ООО «Апиценна», г. Москва e-mail: ov_petrova@apicenna.ru
Сайтханов Э. О., кандидат биологических наук, заведующий кафедрой ветеринарно-санитарной экспертизы, хирургии, акушерства и внутренних болезней животных ФГБОУ ВО «Рязанский агротехнологический университет им. П.А. Костычева», г. Рязань, e-mail: elmanrzn@gmail.com
Ключевые слова: лекарственный препарат, переносимость, кошки, ГАБИТАБС, клинический статус, морфологические показатели, биохимические показатели
Резюме. В настоящем исследовании была проведена оценка переносимости лекарственного препарата для ветеринарного применения ГАБИТАБС в повышенных дозировках.
Установлено, что препарат ГАБИТАБС при однократном пероральном ведении кошкам в дозе 50 мг/кг/сутки (что выше средней терапевтической в 4-5 раз), а также при многократном введении в дозе 20 мг/кг/сутки (а 2 раза выше средней терапевтической для животного) и 30 мг/кг/сутки (в 3 раза выше терапевтической для животного) в течение 28 дней не вызывает функциональных, морфологических нарушений, а также интоксикационного синдрома и удовлетворительно переносится кошками разных пород и пола.
Study of the tolerability of the drug for veterinary use gabitabs on cats
Shantyz A.Kh.1, Lysenko Yu. A.1, Kostyanko N.O.1, Hahov L.A.1, Petrova O.V.2, Sajthanov E. O.3
1Kuban State Agrarian University named after I. T. Trubilin, Krasnodar
2Ltd «Apicenna», Moscow
3Ryazan Agrotechnological University named after P.A. Kostychev, Ryazan
Keywords: drug, tolerance, cats, gabapentin, clinical status, morphological parameters, biochemical parameters
Abstract. In the present study, the tolerability of a medicinal product for veterinary use of GABITABS at higher dosages was assessed.
It has been established that the drug GABITABS with a single oral administration to cats at a dose of 50 mg/kg/day (which is 4-5 times higher than the average therapeutic dose), as well as with repeated administration at a dose of 20 mg/kg/day (and 2 times higher than the average therapeutic for an animal) and 30 mg/kg/day (3 times higher than therapeutic for an animal) for 28 days does not cause functional, morphological disorders, as well as intoxication syndrome and is satisfactorily tolerated by cats of different breeds and gender.
Для цитирования / For citation
Изучение переносимости лекарственного препарата для ветеринарного применения габитабс на кошках / Шантыз А. Х. [и др.] // Ветеринария и кормление. – 2022.
Study of the tolerability of the drug for veterinary use gabitabs on cats / Shantiz A.Kh. [et al.] // Veterinaria I kormlenie. – 2022.
Введение
Действующим веществом нового препарата ГАБИТАБС является габапентин. Он относится к группе противосудорожных средств, обладает анксиолитической активностью, уменьшает боль. Вещество представляет собой конформационно ограниченный аналог гамма-аминомасляной кислоты (ГАМК). Габапентин хорошо проходит через гематоэнцефалический барьер, блокирует кальций-зависимые каналы, ингибирует альфа-2-дельта (α2δ) субъединицу кальциевого канала N-типа на нейронах. Благодаря ингибированию этих каналов, он уменьшает приток кальция, необходимого для высвобождения нейромедиаторов из пресинаптических нейронов. Блокирование кальциевых каналов мало влияет на нормальные нейроны, но может подавлять стимулированные нейроны, участвующие в судорожной активности и боли. В высоких дозах габапентин обладает седативным действием. Основные нежелательные эффекты габапентина у кошек связаны с развитием угнетения и седации. Мировая практика применения габапентина у кошек характеризует достаточно низкий риск развития осложнений при его применении, в том числе при длительных курсах более 1 мес.
Целью настоящего исследования являлось определение переносимости нового лекарственного препарата для ветеринарного применения ГАБИТАБС на кошках.
Материалы и методы
Изучение переносимости нового разрабатываемого в РФ препарата на основе габапентина было проведено в научно-испытательном центре токсико-фармакологических исследований и разработки лекарственных средств ветеринарного применения, кормовых добавок и дезинфектантов (НИЦ Ветфармбиоцентр), которое является структурным подразделением ФГБОУ ВО «Кубанский государственный аграрный университет имени И. Т. Трубилина».
Объект исследования – препарат габапентин (фирменное наименование ГАБИТАБС), разработанный ООО «АПИ-САН» (Россия), в форме таблеток для перорального приема, с содержанием активного вещества 50 мг/таб. Для животных препарат показан для устранения поведенческих расстройств, повышенной тревожности, в том числе при проведении диагностических исследований, посещении мероприятий и ветеринарных учреждений.
В исследовании на основании критериев включения были взяты клинически здоровые животные, весом 4,0 ± 1,2 кг в возрасте от 2 до 4 лет. После обследования животные были размещены в индивидуальный клеточный вольер стационара института. Кормление, уход и содержание животных в эксперименте было стандартизированным, применение других лекарственных средств исключалось.
Для изучения переносимости препарата в различных дозировках в исследование было включено 18 беспородных кошек, которых по принципу аналогов распределили в три группы. Схема применения препарата была следующей:
· 1-я опытная: ГАБИТАБС по 20 мг/кг/в сутки 28 дней.
· 2-я опытная: ГАБИТАБС по 30 мг/кг/в сутки 28 дней.
· 3-я опытная: ГАБИТАБС по 50 мг/кг/однократно.
Препарат животным применяли в одно и тоже время в утренние часы, введение проводили на корень языка при помощи таблеткодавателя.
У животных изучалась динамика массы тела, частоты пульса и дыхания, а также общая температура тела [2, 3]. Оценивали аппетит, поведение, дефекацию и диурез подопытных кошек путем визуального клинического наблюдения. Отбор проб биоматериала (клинической крови и сыворотки) проводили по стандартной методике, оценивая изменения показателей на 0, 3-е (3-я опытная группа), 15-е, 29-е, 38-е сутки от начала исследования. Морфологические показатели крови включали: лейкоциты, эритроциты, тромбоциты, гематокрит, гемоглобин, СОЭ, подсчет лейкоцитарной формулы. Биохимические показатели: АЛТ, АСТ, ЩФ, мочевина, глюкоза, креатинин, альбумин, общий белок, общий билирубин, ГГТ. Полученные данные по гематологическим исследованиям сравнивали со значниями до начала терапии животных и с референсными показатели для вида [1, 4].
Полученные цифровые значения подвергались обработке методами параметрической статистики [5] с использованием программного обеспечения: Microsoft Office Excel 2013 в операционной системе Windows 10. Результаты считали достоверными при уровне вероятности P ≤ 0,05.
Результаты исследований
Во время исследования у подопытных кошек не было отмечено грубых нарушений жизнедеятельности, летальных исходов, проявлений острой токсичности не выявлено. Состояние кожи, цвет слизистых оболочек, размягчения стула не отмечали. В первое применение у отдельных животных наблюдали атаксию у отдельных животных, которая проявлялись через 30–60 мин после введения препарата и длились от 2-х до 7-и часов. У кошек при введении 30 мг/кг/сутки была отмечена гиперсомния.
У пяти кошек 3-й опытной группы после введения препарата наблюдались признаки атаксии длительностью от 4-х до 7-и часов. У 2-х кошек через 1 час после ведения препарата наблюдалась тахикардия и тахипноэ, длительностью от 2 ч. 40 мин. до 3 ч. 15 мин.
Колебания температуры тела (Рис. 1) у кошек всех групп не имели существенных различий и находились на уровне 38,6-39,0 °С.
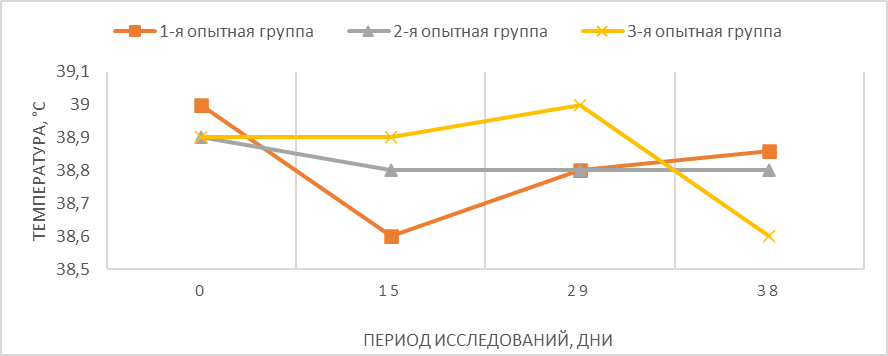
Рисунок 1 – Динамика температуры тела у экспериментальных кошек
При изучении частоты сердечных сокращений (Рис. 2) выявлено, что за период исследований наблюдалось снижение показателей с начала исследования во всех опытных группах, что вероятно связано с адаптацией животных к условиям содержания за счет устранения тревожности на габапентине.
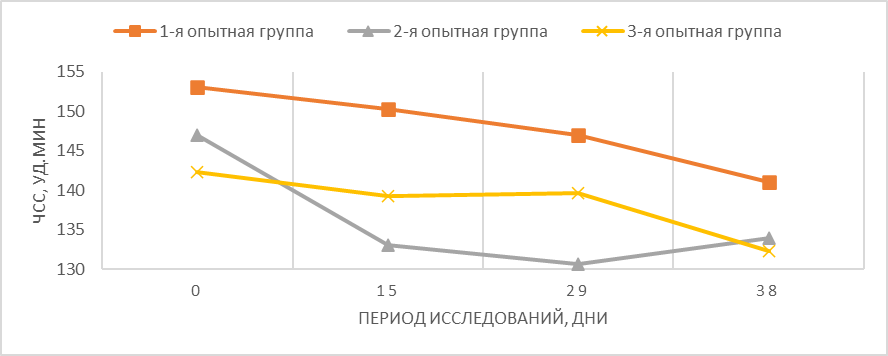
Рисунок 2 – Динамика частоты сердечных сокращений у кошек подопытных групп
При изучении динамики частоты дыхательных движений (Рис. 3) было отмечено повышение среднего значения по группам на 0-й день эксперимента. Вероятны индивидуальные реакции животных на стресс на этапе начала исследования. В дальнейшем показатели снижались и приходили к клинической норме.
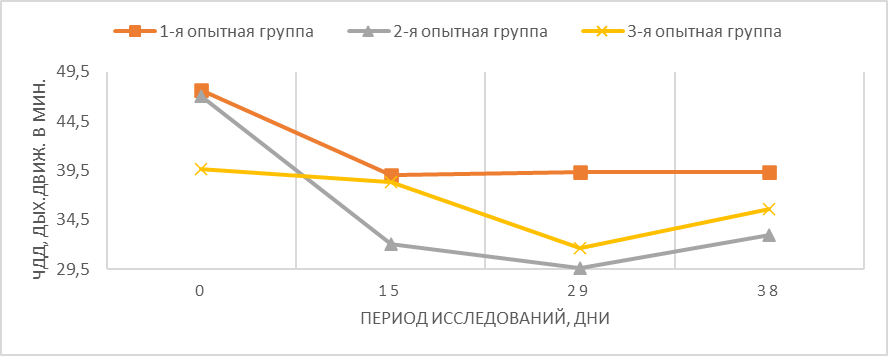
Рисунок 3 – Динамика частоты дыхательных движений подопытных кошек
Влияние высоких доз габапентина на вес животных (Рис. 4) были оценены в эксперименте в динамике. На графике видно, что масса тела кошек не претерпевала значимых статистически изменений.
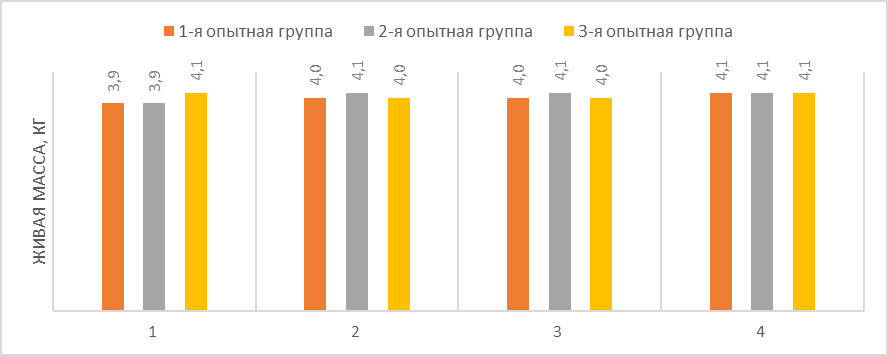
Рисунок 4 – Динамика средней живой массы тела подопытных кошек, при введении препарата Габитабс (1 - 0-е сутки; 2 - 15-е сутки; 3 - 29-е сутки; 4 - 38-е сутки)
Ключевым критерием безопасности препарата является не только отсутствие симптомов и интоксикации, но и отсутствие негативного влияния на гомеостаз, белковый, липидный, углеводный обмен в организме животных. С этой целью был проведен морфологический и биохимический анализ крови животных в разные дни исследования до и после дачи ГАБИТАБСА.
Исследуемый препарат ГАБИТАБС в повышенных дозах не влиял на морфологические свойства крови, не оказывал угнетающего действия на лейко- и эритропоэз. Показатели крови не претерпевали существенных изменений с момента первого контроля (до дачи препарата) вплоть до измерений, выполненных в периоде постнаблюдений. Лейкоцитарная формула подопытных животных как до применения габапентина, так и после не выявила каких-либо ядерных сдвигов, эозинофилии и базофилии не проявлялось, а значит сенсибилизация отсутствовала.
При анализе динамики показателей крови было выявлено ряд тенденций. Так у кошек, получавших исследуемый препарат в дозировке 20 мг/кг/сут, было отмечено постепенное увеличение содержания лейкоцитов на 0,9 %, 11,4 %, 15,2 % относительно фоновых измерений (до дачи препарата). Содержание эритроцитов в конце исследования снизилось на 14,3 % относительно фоновых измерений, однако на 15-й день эксперимента данный показатель увеличился на 2,9 % относительно 0-го дня опыта. Также было отмечено снижение количества тромбоцитов в цельной крови к концу опыта на 5,1 %. Уровень гемоглобина на 15-й день опыта повысился на 2,6 % относительно фоновых измерений, к концу эксперимента его содержание составило 133,66±2,31 г/л, что на 1,2 % выше результатов, полученных на 0-й день эксперимента.
Во 2-й группе кошек, получавших ГАБИТАБС в дозе 30 мг/кг/сут уровень лейкоцитов на 0-й день эксперимента составил 10,77±0,56 тыс/мкл и постепенно увеличивался к концу эксперимента, составив на 39-й день 11,79±0,68 тыс/мкл. Уровень эритроцитов при фоновом измерении составил 7,80±0,58 млн/мкл, на 15-й день 6,63±0,39 млн/мкл, что ниже фонового показателя на 15,0 %, к концу опыта содержание эритроцитов в крови было ниже фоновых показателей на 7,5 %. Также было отмечено увеличение содержания в крови тромбоцитов и гематокрита к концу опыта на 4,3 % и 8,1 % соответственно. Скорость оседания эритроцитов на 0-й день эксперимента составила 7,33±0,95 мм/час, на 15-й и 38-й дни данный показатель снизился на 9,1 % и 6,8 % соответственно, в конце эксперимента СОЭ составила 7,66±0,42 мм/час, что на 4,5 % выше фонового показателя.
В 3-й опытной группе кошек, получивших однократную повышенную дозу препарата Габитабс (50 мг/кг/сут), было отмечено повышение уровня лейкоцитов на 3-й день эксперимента на 1,7 %, относительно фоновых значений. Уровень тромбоцитов: на 3-й день опыта был ниже фоновых измерений на 6,0 %. В показателях гематокрита и СОЭ на 3-й день опыта отмечено снижение относительно измерений на 0-й день эксперимента на 5,6 % и 17,8 % соответственно. Все измеряемые показатели по клинической крови показаны в таблицах 1 и 2.
|
Таблица 1. Результаты общего анализа крови подопытных кошек Table 1. Clinical blood assay of experimental cats |
||||||
|
Показатель |
0-й день |
3-й день |
15-й день |
|||
|
Опытная группа |
Опытная группа |
Опытная группа |
||||
|
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
3-я 50 мг/кг/сут |
3-я 50 мг/кг/сут |
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
|
|
Лейкоциты, тыс/мкл |
10,11±0,64 |
10,77±0,56 |
11,83±1,12 |
12,04±0,78 |
10,20±0,62 |
10,75±1,21 |
|
Эритроциты, млн/мкл |
8,14±0,36 |
7,80±0,58 |
7,34±0,59 |
6,35±0,34 |
8,38±0,45 |
6,63±0,39 |
|
Тромбоциты, тыс/мкл |
296,33±56,45 |
317,00±14,74 |
279,00±22,62 |
262,16±13,412 |
279,83±10,54 |
289,50±10,74 |
|
Гематокрит, % |
34,16±2,81 |
30,78±1,88 |
33,48±2,38 |
31,60±1,78 |
32,97±2,63 |
32,63±2,23 |
|
Гемоглобин, г/л |
132,0±3,33 |
130,83±1,95 |
134,83±2,44 |
136,16±3,30 |
135,50±1,83 |
131,33±1,83 |
|
СОЭ, мм/час |
7,16±0,60 |
7,33±0,95 |
7,50±0,84 |
6,16±0,47 |
6,33±0,49 |
6,66±0,71 |
|
Лейкоцитарная формула: Лимфоциты, % |
47,16±1,66 |
42,50±1,60 |
41,16±0,94 |
44,66±1,22 |
47,66±1,33 |
46,66±2,62 |
|
Сегментоядерные нейтрофилы, % |
41,50±1,56 |
42,33±1,94 |
42,83±1,35 |
42,83±1,07 |
39,16±1,51 |
38,16±3,02 |
|
Палочкоядерные нейтрофилы, % |
4,33±0,42 |
5,66±0,42 |
5,50±0,56 |
5,83±0,40 |
5,66±0,55 |
6,00±0,57 |
|
Юные нейтрофилы, % |
0,66±0,21 |
0,16±0,16 |
0,50±0,22 |
0,33±0,21 |
0,00±0,00 |
0,33±0,21 |
|
Базофилы, % |
0,66±0,21 |
0,33±0,21 |
0,83±0,16 |
0,16±0,16 |
0,00±0,00 |
0,33±0,21 |
|
Моноциты, % |
3,00±0,77 |
4,00±0,36 |
3,66±0,42 |
2,33±0,422 |
3,00±0,57 |
3,33±0,42 |
|
Эозинофилы, % |
2,66±0,66 |
5,00±0,85 |
5,50±0,71 |
3,83±0,47 |
4,50±0,42 |
5,16±0,54 |
|
Таблица 2. Результаты общего анализа крови подопытных кошек (продолжение) Table 2. Clinical blood assay of experimental cats (Table continued) |
||||
|
Показатель |
29-й день |
38-й день |
||
|
Опытная группа |
Опытная группа |
|||
|
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
|
|
Лейкоциты, тыс/мкл |
11,26±0,81 |
11,13±0,51 |
11,65±0,76 |
11,79±0,68 |
|
Эритроциты, млн/мкл |
7,60±0,52 |
6,72±0,64 |
6,97±0,19 |
7,21±0,31 |
|
Тромбоциты, тыс/мкл |
281,16±10,54 |
279,00±19,81 |
277,33±16,48 |
291,16±9,41 |
|
Гематокрит, % |
37,87±1,71 |
34,60±2,06 |
36,21±2,53 |
33,29±1,58 |
|
Гемоглобин, г/л |
134,33±2,66 |
133,00±2,33 |
133,66±2,31 |
132,16±2,77 |
|
СОЭ, мм/час |
6,00±0,44 |
6,83±0,65 |
7,50±0,42 |
7,66±0,42 |
|
Лейкоцитарная формула: Лимфоциты, % |
43,33±2,29 |
43,66±1,60 |
44,16±1,79 |
45,66±1,43 |
|
Сегментоядерные нейтрофилы, % |
43,66±1,40 |
42,66±1,68 |
40,83±2,21 |
40,66±1,66 |
|
Палочкоядерные нейтрофилы, % |
5,33±1,30 |
4,50±0,95 |
6,66±0,55 |
5,50±0,76 |
|
Юные нейтрофилы, % |
0,33±0,21 |
0,16±0,16 |
0,16±0,16 |
0,16±0,13 |
|
Базофилы, % |
0,33±0,21 |
0,66±0,21 |
0,33±0,21 |
0,16±0,16 |
|
Моноциты, % |
3,33±0,71 |
4,00±0,85 |
3,00±0,63 |
3,33±0,76 |
|
Эозинофилы, % |
3,66±0,91 |
4,33±0,61 |
4,83±0,47 |
4,50±0,56 |
Нами были оценены биохимические параметры (табл. 3, 4) в динамике до и после перорального введения препарата в повышенных дозах. Изменение биохимических параметров показывает степень негативного влияния вещества при всасывании в кровь на обмен веществ, функции внутренних органов.
У кошек не было значимой разницы в содержании общего билирубина, АСТ, АЛТ, мочевины, креатинина, общего белка, альбумина, глюкозы, ЩФ, ГГТ. Показатели крови во все дни измерений не превышали референсные.
|
Таблица 3. Результаты биохимического анализа сыворотки подопытных кошек Table 3. Biochemical assay of experimental cats |
||||||
|
Показатель |
0-й день |
3-й день |
15-й день |
|||
|
Опытная группа |
Опытная группа |
Опытная группа |
||||
|
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
3-я 50 мг/кг/сут |
3-я 50 мг/кг/сут |
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
|
|
АЛТ, Ед/л |
32,95±2,85 |
39,61±5,21 |
42,66±2,22 |
40,76±1,75 |
30,56±2,06 |
36,83±3,79 |
|
АСТ, Ед/л |
19,03±1,81 |
21,05±3,88 |
23,56±2,55 |
22,86±1,74 |
15,11±1,20 |
18,85±2,04 |
|
ЩФ, Ед/л |
49,16±3,97 |
55,88±4,43 |
54,41±4,71 |
53,05±3,42 |
42,55±3,47 |
52,91±3,05 |
|
Мочевина, ммоль/л |
8,05±0,30 |
9,51±0,38 |
7,53±0,53 |
8,39±0,41 |
7,38±0,27 |
8,21±0,28 |
|
Глюкоза, ммоль/л |
5,15±0,28 |
5,97±0,20 |
5,43±0,31 |
6,12±0,25 |
5,01±0,14 |
5,40±0,17 |
|
Креатинин, мкмоль/л |
144,03±4,53 |
148,42±5,12 |
142,52±7,25 |
145,14±2,77 |
135,51±2,60 |
130,90±3,09 |
|
Альбумин, г/л |
26,82±1,84 |
30,13±1,86 |
29,38±1,70 |
28,70±0,68 |
29,58±1,54 |
30,36±0,93 |
|
Общий белок, г/л |
62,72±1,83 |
58,13±1,81 |
57,59±1,26 |
59,35±1,08 |
59,39±1,46 |
60,07±1,45 |
|
Общий билирубин, мкмоль/л |
6,20±0,40 |
6,95±0,46 |
6,39±0,57 |
5,60±0,33 |
5,64±0,34 |
6,34±0,35 |
|
ГГТ, Ед/л |
3,20±0,18 |
3,08±0,11 |
2,90±0,11 |
3,21±0,13 |
3,20±0,11 |
3,10±0,26 |
|
Таблица 4. Результаты биохимического анализа сыворотки подопытных кошек (продолжение) Table 4. Biochemical assay of experimental cats (Table continued) |
||||
|
Показатель |
29-й день |
38-й день |
||
|
Опытная группа |
Опытная группа |
|||
|
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
1-я 20 мг/кг/сут |
2-я 30 мг/кг/сут |
|
|
АЛТ, Ед/л |
30,51±2,70 |
29,46±2,77 |
31,23±2,13 |
31,35±1,55 |
|
АСТ, Ед/л |
16,53±1,48 |
15,68±1,60 |
15,80±1,22 |
16,93±0,91 |
|
ЩФ, Ед/л |
42,01±1,80 |
41,46±1,69 |
44,51±3,00 |
39,76±2,40 |
|
Мочевина, ммоль/л |
6,70±0,26 |
6,81±0,21 |
6,47±0,53 |
6,76±0,44 |
|
Глюкоза, ммоль/л |
5,30±0,19 |
5,71±0,33 |
5,83±0,46 |
5,59±0,53 |
|
Креатинин, мкмоль/л |
132,97±1,61 |
137,89±4,39 |
134,79±3,35 |
139,85±3,36 |
|
Альбумин, г/л |
30,33±1,16 |
30,15±1,54 |
30,69±1,14 |
30,39±1,33 |
|
Общий белок, г/л |
60,34±1,33 |
61,75±0,75 |
62,63±1,97 |
62,48±1,25 |
|
Общий билирубин, мкмоль/л |
5,68±0,12 |
5,73±0,15 |
5,82±0,51 |
6,18±0,50 |
|
ГГТ, Ед/л |
3,23±0,19 |
2,98±0,21 |
3,13±0,25 |
2,93±0,14 |
При анализе биохимических показателей крови были определены отдельные тенденции, которые в целом не характеризовали наличие интоксикации у экспериментальных кошек.
У кошек, получавших препарат ГАБИТАБС в дозе 20 мг/кг/сут (1-я опытная группа) были отмечены следующие изменения: показатель аланинаминотрансфераз к концу эксперимента снизился на 5,2 %, аспартатаминотрансфераз на 15-й день опыта был ниже на 20,6 % относительно данных фонового исследования, на 29-й день данный показатель снизился на 13,1 %, к концу опыта на 16,9 %. Среднегрупповой показатель щелочной фосфатазы на 15-й день снизился на 13,4 %, к концу опыта изменения с фоновыми показателями составили 9,4 %. Уровень мочевины в течение опыта постепенно снижался на 8,3 %-19,6 %. Также отметили изменение содержания в сыворотке крови альбуминов: в конце опыта прирост относительно фоновых показателей составил 14,4 %.
Во 2-й опытной группе были отмечены снижение АЛТ на 20,8 % к концу опыта, АСТ на 19,5 %, постепенное снижение показателя щелочной фосфатазы на 5,3 %, 25,8 % и 28,8 % соответственно контрольным точкам опыта. Уровень креатинина к концу эксперимента снизился на 5,7 % относительно фоновых измерений. Показатели общего белка на 39-й день опыта были выше относительно показателей на 0-й день опыта на 7,5 %.
Анализ биохимических показателей сыворотки крови кошек 3-й опытной группы не выявил достоверных различий в исследуемых показателях. Были отмечены изменения в показателях АЛТ: при фоновом измерении на 0-й день опыта составила 42,66±2,22 Ед/л, на 3-й день эксперимента данный показатель был зафиксирован на 40,76±1,75 Ед/л, что на 4,4 % ниже фонового показателя. Аналогичные изменения отмечены в динамике аспартатаминотрансфераз и щелочной фосфатазы: на 3-й день эксперимента данный показатель снизился относительно фоновых измерений на 2,9 %. Уровень мочевины на 3-й день опыта поднялся с 7,53±0,53 ммоль/л до 8,39±0,41 ммоль/л. Также было отмечено увеличение ГГТ в контрольных точках измерения на 10,6 %.
Заключение
Результаты длительного применения препарата ГАБИТАБС не показали развитие токсичности у домашних кошек. Угнетения, рвоты, диареи, подъема температуры, лихорадки не наблюдалось. При применении препарата в дозе в 5 раз выше средней терапевтической однократно также не выявлено нарушений. Вес, аппетит, состояние слизистых оболочек не имели патологических отклонений. После применения у некоторых кошек наблюдалось самопроходящая атаксия, сонливость, что связано с особенностями воздействия габапентина на рецепторы ЦНС.
Литература
1) Бурмистров, Е. Н. Лабораторная диагностика. – М. : «ШАНС БИО», 2021. – 322 с.1
2) Воронин, Е. С. Клиническая диагностика с рентгенологией / Е. С. Воронин, Г. В. Сноз, М. Ф. Васильев и др. –М.: Колос, 2006. – 509 с.2
3) Воронин, Е. С. Практикум по клинической диагностике с рентгенологией / Е. С. Воронин и др. – М. ИНФРА – М, 2014. – 355 с.3
4) Кесарева, Е. А. Клиническая интерпретация биохимических показателей сыворотки крови собак и кошек / Е. А. Кесарева, В. Н. Денисенко. – М.: Колос, 2011. – 26 с.6
5) Лакин Г.Ф. Биометрия. Учебное пособие для биол. Спец. Вузов 4-е изд., перераб. и доп. // Г. Ф. Лакин. – М.: Высшая школа, 1990. – 352 с.7
References
1) Burmistrov, E. N. Laboratornaya diagnostika – M. : «SHANS BIO», 2021. – 322 s.
2) Voronin, E. S. Klinicheskaya diagnostika s rentgenologiej / E. S. Voronin, G. V. Snoz, M. F. Vasil'ev i dr. // - M.: Kolos, 2006. – 509 s.
3) Voronin E. S. Praktikum po klinicheskoj diagnostike s rentgenologiej / E. S. Voronin i dr. // - M. INFRA – M, 2014. – 355 s.
4) Kesareva E. A., Denisenko V. N. Klinicheskaya interpretaciya biohimicheskih pokazatelej syvorotki krovi sobak i koshek / E. A. Kesareva, V. N. Denisenko // - M.: Kolos, 2011. – 26 s.
5) Lakin G.F. Biometriya. Uchebnoe posobie dlya biol. Spec. Vuzov 4-e izd., pererab. i dop. // G. F. Lakin. – M.: Vysshaya shkola, 1990. - 352 s.



